Виды инсулина, его действие и способы введения
Содержание
- Историческая справка
- Механизм действия
- Фармакологические эффекты инсулина
- Фармакокинетика
- Классификация
- Группы инсулинов
- Показания
- Противопоказания
- Применение при беременности
- Осложнения инсулинотерапии. Гипогликемия
- Виды инсулина
- Специфические свойства
- Инъекции
- Рекомендации по хранению
- Строение, изготовление и очистка
- Виды препаратов по источнику получения
- Концентрация
- рН инсулинового раствора
- Какие препараты инсулина лучше применять?
- Факторы, влияющие на всасывание
- Традиционные инъекции
- Современные методы введения
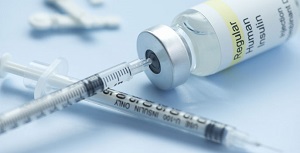 Причиной сахарного диабета 1 типа являются нарушения в работе иммунной системы. Вследствие этих нарушений организм совершает автоагрессию и уничтожает собственные здоровые клетки поджелудочной железы. Она перестает производить инсулин, который теперь должен поставляться извне.
Причиной сахарного диабета 1 типа являются нарушения в работе иммунной системы. Вследствие этих нарушений организм совершает автоагрессию и уничтожает собственные здоровые клетки поджелудочной железы. Она перестает производить инсулин, который теперь должен поставляться извне.
Не все знают, что задачей инсулина является не только снижение уровня сахара в крови. Это ключевое для нашего здоровья вещество участвует в метаболизме белков, углеводов и жиров. Вследствие его работы печень снижает освобождение и повышает поглощение глюкозы, ограничивает выработку мочевины и повышает поглощение фосфатов и калия из крови.
Ключевая роль инсулина в регулировке уровня сахара в крови. Именно он позволяет глюкозе проникать в клетки организма, снабжая их необходимой энергией. Являясь своего рода транспортером, инсулин наполняет глюкозой мышцы, жировые клетки и печень.
Когда уровень инсулина слишком низкий, глюкоза не может попасть в клетки организма. Накапливаясь в крови, она вызывает гипергликемию – очень опасный для организма избыток сахара в крови. Если же уровень инсулина слишком высокий, происходит падение уровня сахара, т.е. гипогликемия.
Инсулин влияет также на работу яичников, улучшает транспорт аминокислот к клеткам и тормозит катаболизм (распад) белков. Это особенно важный гормон для всех, кто мечтает о красивой, рельефной мышечной ткани. Еще одна функция инсулина это улучшение транспорта калия внутрь клеток, а также возможность накопления магния.
Познакомьтесь со статьями, которые я нашел в интернете по теме инсулина, его видов и способов введения.
Инсулин (от лат. insula — островок) является белково-пептидным гормоном, вырабатываемым β-клетками островков Лангерганса поджелудочной железы. В физиологических условиях в β-клетках инсулин образуется из препроинсулина — одноцепочечного белка-предшественника, состоящего из 110 аминокислотных остатков. После переноса через мембрану шероховатого эндоплазматического ретикулума от препроинсулина отщепляется сигнальный пептид из 24 аминокислот и образуется проинсулин. Длинная цепь проинсулина в аппарате Гольджи упаковывается в гранулы, где в результате гидролиза отщепляются четыре основных аминокислотных остатка с образованием инсулина и С-концевого пептида (физиологическая функция С-пептида неизвестна).
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Молекула инсулина состоит из двух полипептидных цепей. Одна из них содержит 21 аминокислотный остаток (цепь А), вторая — 30 аминокислотных остатков (цепь В). Цепи соединены двумя дисульфидными мостиками. Третий дисульфидный мостик сформирован внутри цепи А. Общая молекулярная масса молекулы инсулина — около 5700. Аминокислотная последовательность инсулина считается консервативной. У большинства видов имеется один ген инсулина, кодирующий один белок. Исключение составляют крысы и мыши (имеют по два гена инсулина), у них образуются два инсулина, отличающиеся двумя аминокислотными остатками В-цепи.
Первичная структура инсулина у разных биологических видов, в т.ч. и у различных млекопитающих, несколько различается. Наиболее близкий к структуре инсулина человека — свиной инсулин, который отличается от человеческого одной аминокислотой (у него в цепи В вместо остатка аминокислоты треонина содержится остаток аланина). Бычий инсулин отличается от человеческого тремя аминокислотными остатками.
Историческая справка
 В 1921 г. Фредерик Г. Бантинг и Чарльз Г. Бест, работая в лаборатории Джона Дж. Р. Маклеода в Университете Торонто, выделили из поджелудочной железы экстракт (как позже выяснилось, содержащий аморфный инсулин), который снижал уровень глюкозы в крови у собак с экспериментальным сахарным диабетом. В 1922 г. экстракт поджелудочной железы ввели первому пациенту — 14-летнему Леонарду Томпсону, больному диабетом, и тем самым спасли ему жизнь. В 1923 г. Джеймс Б. Коллип разработал методику очистки экстракта, выделяемого из поджелудочной железы, что в дальнейшем позволило получать из поджелудочных желез свиней и крупного рогатого скота активные экстракты, дающие воспроизводимые результаты.
В 1921 г. Фредерик Г. Бантинг и Чарльз Г. Бест, работая в лаборатории Джона Дж. Р. Маклеода в Университете Торонто, выделили из поджелудочной железы экстракт (как позже выяснилось, содержащий аморфный инсулин), который снижал уровень глюкозы в крови у собак с экспериментальным сахарным диабетом. В 1922 г. экстракт поджелудочной железы ввели первому пациенту — 14-летнему Леонарду Томпсону, больному диабетом, и тем самым спасли ему жизнь. В 1923 г. Джеймс Б. Коллип разработал методику очистки экстракта, выделяемого из поджелудочной железы, что в дальнейшем позволило получать из поджелудочных желез свиней и крупного рогатого скота активные экстракты, дающие воспроизводимые результаты.
В 1923 г. Бантинг и Маклеод за открытие инсулина были удостоены Нобелевской премии по физиологии и медицине. В 1926 г. Дж. Абель и В. Дю-Виньо получили инсулин в кристаллическом виде. В 1939 г. инсулин был впервые одобрен FDA (Food and Drug Administration). Фредерик Сэнгер полностью расшифровал аминокислотную последовательность инсулина (1949–1954 гг.) В 1958 г. Сэнгеру была присуждена Нобелевская премия за работы по расшифровке структуры белков, особенно инсулина. В 1963 г. был синтезирован искусственный инсулин. Первый рекомбинантный человеческий инсулин был одобрен FDA в 1982 г. Аналог инсулина ультракороткого действия (инсулин лизпро) был одобрен FDA в 1996 г.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
Механизм действия
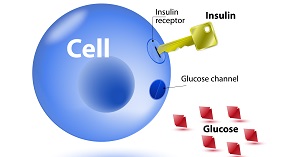 В реализации эффектов инсулина ведущую роль играет его взаимодействие со специфическими рецепторами, локализующимися на плазматической мембране клетки, и образование инсулин-рецепторного комплекса. В комплексе с инсулиновым рецептором инсулин проникает в клетку, где оказывает влияние на процессы фосфорилирования клеточных белков и запускает многочисленные внутриклеточные реакции.
В реализации эффектов инсулина ведущую роль играет его взаимодействие со специфическими рецепторами, локализующимися на плазматической мембране клетки, и образование инсулин-рецепторного комплекса. В комплексе с инсулиновым рецептором инсулин проникает в клетку, где оказывает влияние на процессы фосфорилирования клеточных белков и запускает многочисленные внутриклеточные реакции.
У млекопитающих инсулиновые рецепторы находятся практически на всех клетках — как на классических клетках-мишенях инсулина (гепатоциты, миоциты, липоциты), так и на клетках крови, головного мозга и половых желез. Число рецепторов на разных клетках колеблется от 40 (эритроциты) до 300 тыс. (гепатоциты и липоциты). Рецептор инсулина постоянно синтезируется и распадается, время его полужизни составляет 7–12 ч.
Рецептор инсулина представляет собой крупный трансмембранный гликопротеин, состоящий из двух α-субъединиц с молекулярной массой 135 кДа (каждая содержит 719 или 731 аминокислотный остаток в зависимости от сплайсинга мРНК) и двух β-субъединиц с молекулярной массой 95 кДа (по 620 аминокислотных остатков). Субъединицы соединены между собой дисульфидными связями и образуют гетеротетрамерную структуру β-α-α-β. Альфа-субъединицы расположены внеклеточно и содержат участки, связывающие инсулин, являясь распознающей частью рецептора.
Бета-субъединицы образуют трансмембранный домен, обладают тирозинкиназной активностью и выполняют функцию преобразования сигнала. Связывание инсулина с α-субъединицами инсулинового рецептора приводит к стимуляции тирозинкиназной активности β-субъединиц путем аутофосфорилирования их тирозиновых остатков, происходит агрегация α,β-гетеродимеров и быстрая интернализация гормон-рецепторных комплексов. Активированный рецептор инсулина запускает каскад биохимических реакций, в т.ч. фосфорилирование других белков внутри клетки. Первой из таких реакций является фосфорилирование четырех белков, называемых субстратами рецептора инсулина (insulin receptor substrate), — IRS-1, IRS-2, IRS-3 и IRS-4.
Фармакологические эффекты инсулина
 Инсулин оказывает влияние практически на все органы и ткани. Однако его главными мишенями служат печень, мышечная и жировая ткань.
Инсулин оказывает влияние практически на все органы и ткани. Однако его главными мишенями служат печень, мышечная и жировая ткань.
Эндогенный инсулин — важнейший регулятор углеводного обмена, экзогенный — специфическое сахаропонижающее средство. Влияние инсулина на углеводный обмен связано с тем, что он усиливает транспорт глюкозы через клеточную мембрану и ее утилизацию тканями, способствует превращению глюкозы в гликоген в печени. Инсулин, кроме того, угнетает эндогенную продукцию глюкозы за счет подавления гликогенолиза (расщепление гликогена до глюкозы) и глюконеогенеза (синтез глюкозы из неуглеводных источников — например из аминокислот, жирных кислот ). Помимо гипогликемического, инсулин оказывает ряд других эффектов.
Влияние инсулина на жировой обмен проявляется в угнетении липолиза, что приводит к снижению поступления свободных жирных кислот в кровоток. Инсулин препятствует образованию кетоновых тел в организме. Инсулин усиливает синтез жирных кислот и их последующую эстерификацию.
Инсулин участвует в метаболизме белков: увеличивает транспорт аминокислот через клеточную мембрану, стимулирует синтез пептидов, уменьшает расход тканями белка, тормозит превращение аминокислот в кетокислоты.
Действие инсулина сопровождается активацией или ингибированием ряда ферментов: стимулируются гликогенсинтетаза, пируват-дегидрогеназа, гексокиназа, ингибируются липазы (и гидролизующая липиды жировой ткани, и липопротеин-липаза, уменьшающая «помутнение» сыворотки крови после приема богатой жирами пищи).
В физиологической регуляции биосинтеза и секреции инсулина поджелудочной железой главную роль играет концентрация глюкозы в крови: при повышении ее содержания секреция инсулина усиливается, при снижении — замедляется. На секрецию инсулина, кроме глюкозы, оказывают влияние электролиты (особенно ионы Ca2+), аминокислоты (в т.ч. лейцин и аргинин), глюкагон, соматостатин.
Фармакокинетика
 Препараты инсулина вводят п/к, в/м или в/в (в/в вводят только инсулины короткого действия и только при диабетической прекоме и коме). Нельзя вводить в/в суспензии инсулина. Температура вводимого инсулина должна соответствовать комнатной, т.к. холодный инсулин всасывается медленнее. Наиболее оптимальным способом для постоянной инсулинотерапии в клинической практике является п/к введение.
Препараты инсулина вводят п/к, в/м или в/в (в/в вводят только инсулины короткого действия и только при диабетической прекоме и коме). Нельзя вводить в/в суспензии инсулина. Температура вводимого инсулина должна соответствовать комнатной, т.к. холодный инсулин всасывается медленнее. Наиболее оптимальным способом для постоянной инсулинотерапии в клинической практике является п/к введение.
Полнота всасывания и начало эффекта инсулина зависят от места введения (обычно инсулин вводят в область живота, бедра, ягодицы, верхнюю часть рук), дозы (объема вводимого инсулина), концентрации инсулина в препарате и др.
Скорость всасывания инсулина в кровь из места п/к введения зависит от ряда факторов — типа инсулина, места инъекции, скорости местного кровотока, местной мышечной активности, количества вводимого инсулина (в одно место рекомендуется вводить не более 12–16 ЕД препарата). Быстрее всего инсулин поступает в кровь из подкожной клетчатки передней брюшной стенки, медленнее — из области плеча, передней поверхности бедра и еще медленнее — из подлопаточной области и ягодицы. Это связано со степенью васкуляризации подкожной жировой клетчатки перечисленных областей. Профиль действия инсулина подвержен значительным колебаниям как у различных людей, так и у одного и того же человека.
В крови инсулин связывается с альфа- и бета-глобулинами, в норме — 5–25%, но связывание может возрастать при лечении из-за появления сывороточных антител (выработка антител к экзогенному инсулину приводит к инсулинорезистентности; при использовании современных высокоочищенных препаратов инсулинорезистентность возникает редко). T1/2 из крови составляет менее 10 мин. Большая часть поступившего в кровоток инсулина подвергается протеолитическому распаду в печени и почках. Быстро выводится из организма почками (60%) и печенью (40%); менее 1,5% выводится с мочой в неизмененном виде.
 Препараты инсулина, применяемые в настоящее время, отличаются по ряду признаков, в т.ч. по источнику происхождения, длительности действия, pH раствора (кислые и нейтральные), наличием консервантов (фенол, крезол, фенол-крезол, метилпарабен), концентрацией инсулина — 40, 80, 100, 200, 500 ЕД/мл.
Препараты инсулина, применяемые в настоящее время, отличаются по ряду признаков, в т.ч. по источнику происхождения, длительности действия, pH раствора (кислые и нейтральные), наличием консервантов (фенол, крезол, фенол-крезол, метилпарабен), концентрацией инсулина — 40, 80, 100, 200, 500 ЕД/мл.
Классификация
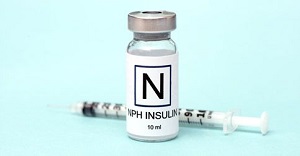 Инсулины обычно классифицируют по происхождению (бычий, свиной, человеческий, а также аналоги человеческого инсулина) и продолжительности действия.
Инсулины обычно классифицируют по происхождению (бычий, свиной, человеческий, а также аналоги человеческого инсулина) и продолжительности действия.
В зависимости от источников получения различают инсулины животного происхождения (главным образом препараты свиного инсулина), препараты инсулина человека полусинтетические (получают из свиного инсулина методом ферментативной трансформации), препараты инсулина человека генно-инженерные (ДНК-рекомбинантные, получаемые методом генной инженерии).
Для медицинского применения инсулин ранее получали в основном из поджелудочных желез крупного рогатого скота, затем из поджелудочных желез свиней, учитывая, что свиной инсулин более близок к инсулину человека. Поскольку бычий инсулин, отличающийся от человеческого тремя аминокислотами, достаточно часто вызывает аллергические реакции, на сегодняшний день он практически не применяется. Свиной инсулин, отличающийся от человеческого одной аминокислотой, реже вызывает аллергические реакции. В лекарственных препаратах инсулина при недостаточной очистке могут присутствовать примеси (проинсулин, глюкагон, соматостатин, белки, полипептиды), способные вызывать различные побочные реакции. Современные технологии позволяют получать очищенные (монопиковые — хроматографически очищенные с выделением «пика» инсулина), высокоочищенные (монокомпонентные) и кристаллизованные препараты инсулина. Из препаратов инсулина животного происхождения предпочтение отдается монопиковому инсулину, получаемому из поджелудочной железы свиней. Получаемый методами генной инженерии инсулин полностью соответствует аминокислотному составу инсулина человека.
Активность инсулина определяют биологическим методом (по способности понижать содержание глюкозы в крови у кроликов) или физико-химическим методом (путем электрофореза на бумаге или методом хроматографии на бумаге). За одну единицу действия, или международную единицу, принимают активность 0,04082 мг кристаллического инсулина. Поджелудочная железа человека содержит до 8 мг инсулина (примерно 200 ЕД).
Препараты инсулина по длительности действия подразделяют на препараты короткого и ультракороткого действия — имитируют нормальную физиологическую секрецию инсулина поджелудочной железой в ответ на стимуляцию, препараты средней продолжительности и препараты длительного действия — имитируют базальную (фоновую) секрецию инсулина, а также комбинированные препараты (сочетают оба действия).
Группы инсулинов
Инсулины ультракороткого действия (гипогликемический эффект развивается через 10–20 мин после п/к введения, пик действия достигается в среднем через 1–3 ч, длительность действия составляет 3–5 ч):
- инсулин лизпро (Хумалог);
- инсулин аспарт (НовоРапид Пенфилл, НовоРапид ФлексПен);
- инсулин глулизин (Апидра).
Инсулины короткого действия (начало действия обычно через 30–60 мин; максимум действия через 2–4 ч; продолжительность действия до 6–8 ч):
- инсулин растворимый [человеческий генно-инженерный] (Актрапид HМ, Генсулин Р, Ринсулин Р, Хумулин Регуляр);
- инсулин растворимый [человеческий полусинтетический] (Биогулин Р, Хумодар Р);
- инсулин растворимый [свиной монокомпонентный] (Актрапид МС, Монодар, Моносуинсулин МК).
Препараты инсулина пролонгированного действия — включают в себя препараты средней продолжительности действия и препараты длительного действия.
Инсулины средней длительности действия (начало через 1,5–2 ч; пик спустя 3–12 ч; продолжительность 8–12 ч):
- инсулин-изофан [человеческий генно-инженерный] (Биосулин Н, Гансулин Н, Генсулин Н, Инсуман Базал ГТ, Инсуран НПХ, Протафан НМ, Ринсулин НПХ, Хумулин НПХ);
- инсулин-изофан [человеческий полусинтетический] (Биогулин Н, Хумодар Б);
- инсулин-изофан [свиной монокомпонентный] (Монодар Б, Протафан МС);
- инсулин-цинк суспензия составная (Монотард МС).
Инсулины длительного действия (начало через 4–8 ч; пик спустя 8–18 ч; общая продолжительность 20–30 ч):
- инсулин гларгин (Лантус);
- инсулин детемир (Левемир Пенфилл, Левемир ФлексПен).
Препараты инсулина комбинированного действия (бифазные препараты) (гипогликемический эффект начинается через 30 мин после п/к введения, достигает максимума через 2–8 ч и продолжается до 18–20 ч):
- инсулин двухфазный [человеческий полусинтетический] (Биогулин 70/30, Хумодар K25);
- инсулин двухфазный [человеческий генно-инженерный] (Гансулин 30Р, Генсулин М 30, Инсуман Комб 25 ГТ, Микстард 30 НМ, Хумулин М3);
- инсулин аспарт двухфазный (НовоМикс 30 Пенфилл, НовоМикс 30 ФлексПен).
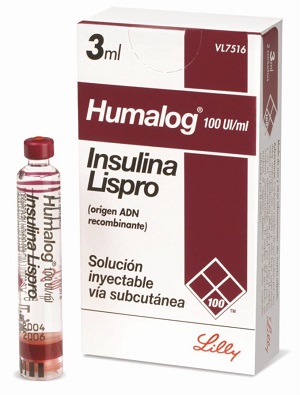 Инсулины ультракороткого действия — аналоги инсулина человека. Известно, что эндогенный инсулин в β-клетках поджелудочной железы, а также молекулы гормона в выпускаемых растворах инсулина короткого действия полимеризованы и представляют собой гексамеры. При п/к введении гексамерные формы всасываются медленно и пик концентрации гормона в крови, аналогичный таковому у здорового человека после еды, создать невозможно.
Инсулины ультракороткого действия — аналоги инсулина человека. Известно, что эндогенный инсулин в β-клетках поджелудочной железы, а также молекулы гормона в выпускаемых растворах инсулина короткого действия полимеризованы и представляют собой гексамеры. При п/к введении гексамерные формы всасываются медленно и пик концентрации гормона в крови, аналогичный таковому у здорового человека после еды, создать невозможно.
Первым коротко действующим аналогом инсулина, который всасывается из подкожной клетчатки в 3 раза быстрее, чем человеческий инсулин, был инсулин лизпро. Инсулин лизпро — производное человеческого инсулина, полученное путем перестановки двух аминокислотных остатков в молекуле инсулина (лизин и пролин в положениях 28 и 29 В-цепи). Модификация молекулы инсулина нарушает образование гексамеров и обеспечивает быстрое поступление препарата в кровь.
Почти сразу после п/к введения в тканях молекулы инсулина лизпро в виде гексамеров быстро диссоциируют на мономеры и поступают в кровь. Другой аналог инсулина — инсулин аспарт — был создан путем замены пролина в положении В28 на отрицательно заряженную аспарагиновую кислоту. Подобно инсулину лизпро, после п/к введения он также быстро распадается на мономеры. В инсулине глулизине замещение аминокислоты аспарагин человеческого инсулина в позиции В3 на лизин и лизина в позиции В29 на глутаминовую кислоту также способствует более быстрой абсорбции. Аналоги инсулина ультракороткого действия можно вводить непосредственно перед приемом пищи или после еды.
Инсулины короткого действия (их называют также растворимыми) — это растворы в буфере с нейтральными значениями pH (6,6–8,0). Они предназначены для подкожного, реже — внутримышечного введения. При необходимости их вводят также внутривенно. Они оказывают быстрое и относительно непродолжительное гипогликемическое действие.
Эффект после подкожной инъекции наступает через 15–20 мин, достигает максимума через 2 ч; общая продолжительность действия составляет примерно 6 ч. Ими пользуются в основном в стационаре в ходе установления необходимой для больного дозы инсулина, а также когда требуется быстрый (ургентный) эффект — при диабетической коме и прекоме. При в/в введении T1/2 составляет 5 мин, поэтому при диабетической кетоацидотической коме инсулин вводят в/в капельно. Препараты инсулина короткого действия применяют также в качестве анаболических средств и назначают, как правило, в малых дозах (по 4–8 ЕД 1–2 раза в день).
Инсулины средней длительности действия хуже растворимы, медленнее всасываются из подкожной клетчатки, вследствие чего обладают более длительным эффектом. Продолжительное действие этих препаратов достигается наличием специального пролонгатора — протамина (изофан, протафан, базал) или цинка. Замедление всасывания инсулина в препаратах, содержащих инсулин цинк суспензию составную, обусловлено наличием кристаллов цинка. НПХ-инсулин (нейтральный протамин Хагедорна, или изофан) представляет собой суспензию, состоящую из инсулина и протамина (протамин — белок, изолированный из молок рыб) в стехиометрическом соотношении.
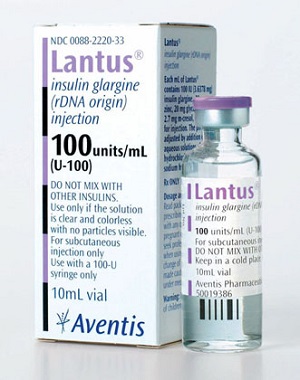 К инсулинам длительного действия относится инсулин гларгин — аналог человеческого инсулина, полученный методом ДНК-рекомбинантной технологии — первый препарат инсулина, который не имеет выраженного пика действия. Инсулин гларгин получают путем двух модификаций в молекуле инсулина: заменой в позиции 21 А-цепи (аспарагин) на глицин и присоединением двух остатков аргинина к С-концу В-цепи. Препарат представляет собой прозрачный раствор с рН 4.
К инсулинам длительного действия относится инсулин гларгин — аналог человеческого инсулина, полученный методом ДНК-рекомбинантной технологии — первый препарат инсулина, который не имеет выраженного пика действия. Инсулин гларгин получают путем двух модификаций в молекуле инсулина: заменой в позиции 21 А-цепи (аспарагин) на глицин и присоединением двух остатков аргинина к С-концу В-цепи. Препарат представляет собой прозрачный раствор с рН 4.
Кислый рН стабилизирует гексамеры инсулина и обеспечивает длительное и предсказуемое всасывание препарата из подкожной клетчатки. Однако из-за кислого рН инсулин гларгин нельзя комбинировать с инсулинами короткого действия, которые имеют нейтральный рН. Однократное введение инсулина гларгина обеспечивает 24-часовой беспиковый гликемический контроль. Большинство препаратов инсулина обладают т.н. «пиком» действия, отмечающимся, когда концентрация инсулина в крови достигает максимума. Инсулин гларгин не обладает выраженным пиком, поскольку высвобождается в кровоток с относительно постоянной скоростью.
Препараты инсулина пролонгированного действия выпускаются в различных лекарственных формах, оказывающих гипогликемический эффект разной продолжительности (от 10 до 36 ч). Пролонгированный эффект позволяет уменьшить число ежедневных инъекций. Выпускаются они обычно в виде суспензий, вводимых только подкожно или внутримышечно. При диабетической коме и прекоматозных состояниях пролонгированные препараты не применяют.
Комбинированные препараты инсулина представляют собой суспензии, состоящие из нейтрального растворимого инсулина короткого действия и инсулина-изофан (средней длительности действия) в определенных соотношениях. Такое сочетание инсулинов разной продолжительности действия в одном препарате позволяет избавить пациента от двух инъекций при раздельном использовании препаратов.
Показания
Основным показанием к применению инсулина является сахарный диабет типа 1, однако в определенных условиях его назначают и при сахарном диабете типа 2, в т.ч. при резистентности к пероральным гипогликемическим средствам, при тяжелых сопутствующих заболеваниях, при подготовке к оперативным вмешательствам, диабетической коме, при диабете у беременных.
Инсулины короткого действия применяют не только при сахарном диабете, но и при некоторых других патологических процессах, например, при общем истощении (в качестве анаболического средства), фурункулезе, тиреотоксикозе, при заболеваниях желудка (атония, гастроптоз), хроническом гепатите, начальных формах цирроза печени, а также при некоторых психических заболеваниях (введение больших доз инсулина — т.н. гипогликемическая кома); иногда он используется как компонент «поляризующих» растворов, используемых для лечения острой сердечной недостаточности.
 Инсулин является основным специфическим средством терапии сахарного диабета. Лечение сахарного диабета проводится по специально разработанным схемам с использованием препаратов инсулина разной продолжительности действия. Выбор препарата зависит от тяжести и особенностей течения заболевания, общего состояния больного и от скорости наступления и продолжительности сахароснижающего действия препарата.
Инсулин является основным специфическим средством терапии сахарного диабета. Лечение сахарного диабета проводится по специально разработанным схемам с использованием препаратов инсулина разной продолжительности действия. Выбор препарата зависит от тяжести и особенностей течения заболевания, общего состояния больного и от скорости наступления и продолжительности сахароснижающего действия препарата.
Все препараты инсулина применяются при условии обязательного соблюдения диетического режима с ограничением энергетической ценности пищи (от 1700 до 3000 ккал).
При определении дозы инсулина руководствуются уровнем гликемии натощак и в течение суток, а также уровнем глюкозурии в течение суток. Окончательный подбор дозы проводится под контролем снижения гипергликемии, глюкозурии, а также общего состояния больного.
Противопоказания
Инсулин противопоказан при заболеваниях и состояниях, протекающих с гипогликемией (например инсулинома), при острых заболеваниях печени, поджелудочной железы, почек, язве желудка и двенадцатиперстной кишки, декомпенсированных пороках сердца, при острой коронарной недостаточности и некоторых других заболеваниях.
Применение при беременности
 Основным медикаментозным методом лечения сахарного диабета во время беременности является инсулинотерапия, которая проводится под тщательным контролем. При сахарном диабете типа 1 продолжают лечение инсулином. При сахарном диабете типа 2 отменяют пероральные гипогликемические средства и проводят диетотерапию.
Основным медикаментозным методом лечения сахарного диабета во время беременности является инсулинотерапия, которая проводится под тщательным контролем. При сахарном диабете типа 1 продолжают лечение инсулином. При сахарном диабете типа 2 отменяют пероральные гипогликемические средства и проводят диетотерапию.
Гестационный сахарный диабет (диабет беременных) — это нарушение углеводного обмена, впервые возникшее во время беременности. Он сопровождается повышенным риском перинатальной смертности, частоты врожденных уродств, а также риском прогрессирования диабета через 5–10 лет после родов. Лечение гестационного сахарного диабета начинают с диетотерапии. При неэффективности диетотерапии применяют инсулин.
Для пациенток с ранее имевшимся или гестационным сахарным диабетом важно в течение всей беременности поддерживать адекватную регуляцию метаболических процессов. Потребность в инсулине может уменьшаться в I триместре беременности и увеличиваться во II–III триместрах. Во время родов и непосредственно после них потребность в инсулине может резко снизиться (возрастает риск развития гипогликемии). В этих условиях существенное значение имеет тщательный контроль содержания глюкозы в крови.
Инсулин не проникает через плацентарный барьер. Однако материнские IgG-антитела к инсулину проходят через плаценту и, вероятно, могут вызывать гипергликемию у плода за счет нейтрализации секретируемого у него инсулина. С другой стороны, нежелательная диссоциация комплексов инсулин–антитело может привести к гиперинсулинемии и гипогликемии у плода или новорожденного. Показано, что переход с препаратов бычьего/свиного инсулина на монокомпонентные препараты сопровождается снижением титра антител. В связи с этим при беременности рекомендуют использовать только препараты инсулина человека.
Аналоги инсулина (как и другие недавно разработанные средства) с осторожностью назначают при беременности, хотя достоверных данных о неблагоприятном воздействии нет. В соответствии с общепризнанными рекомендациями FDA (Food and Drug Administration), определяющими возможность применения ЛС при беременности, препараты инсулинов по действию на плод относятся к категории B (изучение репродукции на животных не выявило неблагоприятного действия на плод, а адекватных и строго контролируемых исследований у беременных женщин не проведено), либо к категории C (изучение репродукции на животных выявило неблагоприятное действие на плод, а адекватных и строго контролируемых исследований у беременных женщин не проведено, однако потенциальная польза, связанная с применением ЛС у беременных, может оправдывать его использование, несмотря на возможный риск). Так, инсулин лизпро относится к классу B, а инсулин аспарт и инсулин гларгин — к классу C.
Осложнения инсулинотерапии. Гипогликемия
Введение слишком высоких доз, а также недостаток поступления с пищей углеводов могут вызвать нежелательное гипогликемическое состояние, может развиться гипогликемическая кома с потерей сознания, судорогами и угнетением сердечной деятельности. Гипогликемия может также развиться в связи с действием дополнительных факторов, которые увеличивают чувствительность к инсулину (например надпочечниковая недостаточность, гипопитуитаризм) или увеличивают захват глюкозы тканями (физическая нагрузка).
К ранним симптомам гипогликемии, которые в значительной степени связаны с активацией симпатической нервной системы (адренергическая симптоматика) относятся тахикардия, холодный пот, дрожь, с активацией парасимпатической системы — сильный голод, тошнота, а также ощущение покалывания в области губ и языка. При первых признаках гипогликемии необходимо проведение срочных мероприятий: больной должен выпить сладкий чай или съесть несколько кусков сахара. При гипогликемической коме в вену вводят 40% раствор глюкозы в количестве 20–40 мл и более, пока больной не выйдет из коматозного состояния (обычно не более 100 мл). Снять гипогликемию можно также внутримышечным или подкожным введением глюкагона.
 Увеличение массы тела при инсулинотерапии связано с устранением глюкозурии, увеличением реальной калорийности пищи, повышением аппетита и стимуляцией липогенеза под действием инсулина. При соблюдении принципов рационального питания этого побочного эффекта можно избежать.
Увеличение массы тела при инсулинотерапии связано с устранением глюкозурии, увеличением реальной калорийности пищи, повышением аппетита и стимуляцией липогенеза под действием инсулина. При соблюдении принципов рационального питания этого побочного эффекта можно избежать.
Применение современных высокоочищенных препаратов гормона (особенно генно-инженерных препаратов человеческого инсулина) относительно редко приводит к развитию инсулинорезистентности и явлениям аллергии, однако такие случаи не исключены. Развитие острой аллергической реакции требует проведения немедленной десенсибилизирующей терапии и замены препарата. При развитии реакции на препараты бычьего/свиного инсулина следует заменить их препаратами инсулина человека. Местные и системные реакции (зуд, локальная или системная сыпь, образование подкожных узелков в месте инъекции) связаны с недостаточной очисткой инсулина от примесей или с применением бычьего или свиного инсулина, отличающихся по аминокислотной последовательности от человеческого.
Самые частые аллергические реакции — кожные, опосредуемые IgE-антителами. Изредка наблюдаются системные аллергические реакции, а также инсулинорезистентность, опосредуемые IgG-антителами.
Нарушение зрения
Преходящие нарушения рефракции глаза возникают в самом начале инсулинотерапии и проходят самостоятельно через 2–3 недели.
Отеки
В первые недели терапии возникают также преходящие отеки ног в связи с задержкой жидкости в организме, т.н. инсулиновые отеки.
К местным реакциям относят липодистрофию в месте повторных инъекций (редкое осложнение). Выделяют липоатрофию (исчезновение отложений подкожного жира) и липогипертрофию (увеличение отложения подкожного жира). Эти два состояния имеют разную природу. Липоатрофия — иммунологическая реакция, обусловленная главным образом введением плохо очищенных препаратов инсулина животного происхождения, в настоящее время практически не встречается.
Липогипертрофия развивается и при использовании высокоочищенных препаратов человеческого инсулина и может возникать при нарушении техники введения (холодный препарат, попадание спирта под кожу), а также вследствие анаболического местного действия самого препарата. Липогипертрофия создает косметический дефект, что является проблемой для пациентов. Кроме того, из-за этого дефекта нарушается всасывание препарата. Для предупреждения развития липогипертрофии рекомендуется постоянно менять места инъекций в пределах одной области, оставляя расстояние между двумя проколами не менее 1 см.
Могут отмечаться такие местные реакции, как боль в месте введения.
Взаимодействие
Препараты инсулина можно комбинировать друг с другом. Многие ЛС могут вызывать гипо- или гипергликемию, либо изменять реакцию больного сахарным диабетом на лечение. Следует учитывать взаимодействие, возможное при одновременном применении инсулина с другими лекарственными средствами.
Альфа-адреноблокаторы и бета-адреномиметики увеличивают секрецию эндогенного инсулина и усиливают действие препарата. Гипогликемическое действие инсулина усиливают пероральные гипогликемические средства, салицилаты, ингибиторы МАО (включая фуразолидон, прокарбазин, селегилин), ингибиторы АПФ, бромокриптин, октреотид, сульфаниламиды, анаболические стероиды (особенно оксандролон, метандиенон) и андрогены (повышают чувствительность тканей к инсулину и увеличивают резистентность тканей к глюкагону, что и приводит к гипогликемии, особенно в случае инсулинорезистентности; может понадобиться снижение дозы инсулина), аналоги соматостатина, гуанетидин, дизопирамид, клофибрат, кетоконазол, препараты лития, мебендазол, пентамидин, пиридоксин, пропоксифен, фенилбутазон, флуоксетин, теофиллин, фенфлурамин, препараты лития, препараты кальция, тетрациклины. Хлорохин, хинидин, хинин снижают деградацию инсулина и могут повышать концентрацию инсулина в крови и увеличивать риск гипогликемии.
 Ингибиторы карбоангидразы (особенно ацетазоламид), стимулируя панкреатические β-клетки, способствуют высвобождению инсулина и повышают чувствительность рецепторов и тканей к инсулину; хотя одновременное использование этих ЛС с инсулином может повышать гипогликемическое действие, эффект может быть непредсказуемым.
Ингибиторы карбоангидразы (особенно ацетазоламид), стимулируя панкреатические β-клетки, способствуют высвобождению инсулина и повышают чувствительность рецепторов и тканей к инсулину; хотя одновременное использование этих ЛС с инсулином может повышать гипогликемическое действие, эффект может быть непредсказуемым.
Целый ряд ЛС вызывают гипергликемию у здоровых людей и усугубляют течение заболевания у больных сахарным диабетом. Гипогликемическое действие инсулина ослабляют: антиретровирусные ЛС, аспарагиназа, пероральные гормональные контрацептивы, глюкокортикоиды, диуретики (тиазидные, этакриновая кислота), гепарин, антагонисты Н2-рецепторов, сульфинпиразон, трициклические антидепрессанты, добутамин, изониазид, кальцитонин, ниацин, симпатомиметики, даназол, клонидин, БКК, диазоксид, морфин, фенитоин, соматотропин, тиреоидные гормоны, производные фенотиазина, никотин, этанол.
Глюкокортикоиды и эпинефрин оказывают на периферические ткани эффект, противоположный инсулину. Так, длительный прием системных глюкокортикоидов может вызывать гипергликемию, вплоть до сахарного диабета (стероидный диабет), который может наблюдаться примерно у 14% пациентов, принимающих системные кортикостероиды в течение нескольких недель или при длительном применении топических кортикостероидов.
Некоторые ЛС ингибируют секрецию инсулина непосредственно (фенитоин, клонидин, дилтиазем) либо за счет уменьшения запасов калия (диуретики). Тиреоидные гормоны ускоряют метаболизм инсулина.
 Наиболее значимо и часто влияют на действие инсулина бета-адреноблокаторы, пероральные гипогликемические средства, глюкокортикоиды, этанол, салицилаты.
Наиболее значимо и часто влияют на действие инсулина бета-адреноблокаторы, пероральные гипогликемические средства, глюкокортикоиды, этанол, салицилаты.
Этанол ингибирует глюконеогенез в печени. Этот эффект наблюдается у всех людей. В связи с этим следует иметь в виду, что злоупотребление алкогольными напитками на фоне инсулинотерапии может привести к развитию тяжелого гипогликемического состояния. Небольшие количества алкоголя, принимаемого вместе с едой, обычно не вызывают проблем.
Бета-адреноблокаторы могут ингибировать секрецию инсулина, изменять метаболизм углеводов и увеличивать периферическую резистентность к действию инсулина, что приводит к гипергликемии. Однако они могут также ингибировать действие катехоламинов на глюконеогенез и гликогенолиз, что сопряжено с риском тяжелых гипогликемических реакций у больных сахарным диабетом.
Более того, любой из бета-адреноблокаторов может маскировать адренергическую симптоматику, вызванную снижением уровня глюкозы в крови (в т.ч. тремор, сердцебиение), нарушая тем самым своевременное распознавание пациентом гипогликемии. Селективные бета1-адреноблокаторы (в т.ч. ацебутолол, атенолол, бетаксолол, бисопролол, метопролол) проявляют эти эффекты в меньшей степени.
НПВС и салицилаты в высоких дозах ингибируют синтез простагландина Е (который ингибирует секрецию эндогенного инсулина) и усиливают таким образом базальную секрецию инсулина, повышают чувствительность β-клеток поджелудочной железы к глюкозе; гипогликемический эффект при одновременном применении может потребовать корректировки дозы НПВС или салицилатов и/или инсулина, особенно при длительном совместном использовании.
Внимание!В настоящее время выпускается значительное число инсулиновых препаратов, в т.ч. полученных из поджелудочных желез животных и синтезированных методами генной инженерии. Препаратами выбора для проведения инсулинотерапии являются генно-инженерные высокоочищенные человеческие инсулины, обладающие минимальной антигенностью (иммуногенной активностью), а также аналоги человеческого инсулина.
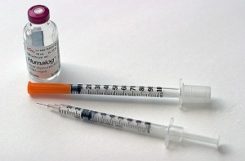
Препараты инсулина выпускаются в стеклянных флаконах, герметически укупоренных резиновыми пробками с алюминиевой обкаткой, в специальных т.н. инсулиновых шприцах или шприц-ручках. При использовании шприц-ручек препараты находятся в специальных флаконах-картриджах (пенфиллах).
Разрабатываются интраназальные формы инсулина и препараты инсулина для приема внутрь. При комбинации инсулина с детергентом и введении в виде аэрозоля на слизистую оболочку носа эффективный уровень в плазме достигается так же быстро, как и при в/в болюсном введении. Препараты инсулина для интраназального и перорального применения находятся на стадии разработки или проходят клинические испытания.
Инсулин – гормон, который вырабатывает поджелудочная железа. Каково химическое строение инсулина? Это – белок, который вырабатывается в бета- клетках поджелудочной железы, а затем выделяется в кровь. Инсулин – основной регулятор углеводного обмена в организме. У людей, больных сахарным диабетом, снижается или прекращается выработка естественного инсулина. Вот почему им требуется введение инсулина, что называется, извне.
Виды инсулина
- Животный инсулин. Его получают из поджелудочных желез животных (свиней и крупного рогатого скота).
- Человеческий инсулин. Его получают генно-инженерным путем. Это синтетический инсулин, который по характеристикам близок к естественному, тому, что вырабатывает человеческий организм.
- Аналоговый инсулин.
В настоящий момент животный инсулин используется гораздо реже, чем человеческий и аналоговый. Человеческий инсулин гораздо предпочтительнее, так как организм не воспринимает его как чужеродное вещество.
Шесть основных типов
- Быстродействующий инсулин. Его применяют непосредственно перед едой, во время приема пищи, или сразу же после еды. Пик его воздействия приходится на первые три часа. Длительность воздействия быстродействующего инсулина не превышает 5 часов. То есть, он актуален для конкретного приема пищи.
- Аналоговый инсулин длительного действия – своеобразны «рекордсмен». Одного приема такого инсулина хватает на сутки. Этот тип инсулина не зависит от приема пищи, благодаря отсутствию пика воздействия.
- Инсулин короткого действия. Его применяют за 15-20 (максимум за 30) минут до очередного приема пищи. Назначение этого вида инсулина – сглаживать процесс возрастания уровня глюкозы в крови, которое происходит после приёма пищи. Пик воздействия инсулина короткого действия приходится на промежуток от 2 до 6 часов после приёма пищи. Время действия – 8 часов.
- Инсулин средней и большой длительности действия. Его применяют два раза в день. Он нужен для поддержания нормального уровня холестерина, в сочетании с инсулином короткого действия или быстродействующим инсулином. Пик действия наступает через 4 часа после еды, а длительность действия достигает 8 часов.
- Смешанный инсулин. Предварительная смесь инсулина короткого и среднего действия
- Смешанный аналоговый инсулин. Это предварительно смешанные два вида инсулина – среднего действия и быстродействующего.
Специфические свойства
Инсулин переваривается и разрушается в кишечнике. Вот почему основной способ введения – подкожные инъекции. Важная особенность инсулина – суточные колебания его концентрации в крови. Существует базальный (постоянный) уровень, а также – пики концентрации. Они связаны с повышением глюкозы в крови, которое наступает после приема пищи. При инсулинотерапии очень важно обеспечить базальный (постоянный) уровень и соблюдать график дополнительных инъекций инсулина перед едой.
Инъекции
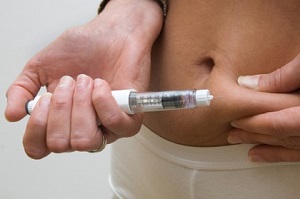 Инсулин вводится подкожно, а не внутримышечно или внутривенно. После инъекции инсулин поступает в кровоток.
Инсулин вводится подкожно, а не внутримышечно или внутривенно. После инъекции инсулин поступает в кровоток.
Для инъекций используются несколько областей: ягодицы, передняя поверхность бедер и живота, наружная поверхность плеч. В некоторых случаях врач рекомендует и другие части тела, к примеру – руки. Особенности инъекции инсулина в том, что он всасывается с разной скоростью из различных областей. Быстрее всего процесс всасывания проистекает, если инъекции делается в область живота.
Место введения инсулина рекомендуется менять, при этом, придерживаясь правила: смена мест для инъекции должна быть одинаковой каждый день. Свободное чередование может привести к колебаниям уровня сахара крови.
 Эффективная терапия не может быть без грамотного и точного расчета доз.
Эффективная терапия не может быть без грамотного и точного расчета доз.
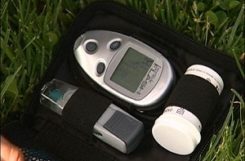
Инсулин выпускается в трех различных формах: флаконы с раствором, шприц-ручки с раствором и набирающие все большую популярность инсулиновые помпы.
При этом, многие не знают, что лечение с помощью инсулиновых помп и шприцов (шприц-ручек) имеет примерно равные показатели эффективности. Выбор в пользу того или иного способа введения инсулина обусловлен факторами цены и психологии. Отметим, что инсулиновая помпа – более современное и технологичное решение, а также – и более комфортное, при достижении привыкания.
Рекомендации по хранению
Любой тип инсулина нужно хранить при температуре от 2 до 25 градусов C. При этом, нужно помнить, что обычная средняя температура в квартире – плюс 25 градусов, но в период летней жары она может серьезно возрастать.
Инсулин, который не предполагается использовать в данный момент, рекомендуется хранить в холодильнике. Там он может находиться до года. Не следует хранить инсулин в морозильной камере, и даже рядом с ней. Помните: замороженный инсулин уже не годен для применения.
Для инсулина, который собираетесь использовать, найдите прохладное сухое место. Вне холодильника можно держать инсулин меньше месяца (до 28 дней). Если инсулин пролежал вне холодильника более этого времени, его следует выбросить.
Инсулин относится к тем немногочисленным, действительно жизнеспасающим лекарствам, которые произвели настоящий переворот в судьбе больных: до получения инсулина в 1922 г. больных инсулинзависимым (“юношеским”) сахарным диабетом ждала неминуемая смерть от диабетической комы в течение одного-двух лет от начала заболевания, несмотря на применение самых фантастических и изнурительных диет.
С момента создания первого препарата прошло более 75 лет, однако до сих пор остаются актуальными, хотя и резкими, сказанные тогда слова пионера диабетологии Э.П. Джослина (США): “Инсулин – лекарство для умных, а не для дураков, будь то врачи или пациенты”. Ему вторит и Дж. Хэрроп, автор первого в мире пособия по инсулинотерапии (1924 г.): “Как часто бывает при появлении новых терапевтических средств, в случае с инсулином мы имеем дело с палкой о двух концах. Если применять его правильно – это благо, а если неправильно – это опасность для больного!
К 1998 г. в России зарегистрировано более 20 препаратов инсулина короткого действия (ИКД) и около 40 препаратов инсулина продленного действия (ИПД). Многолетний опыт консультирования в многопрофильных стационарах заставляет признать, что степень осведомленности врачей-неэндокринологов о свойствах, качественных и количественных различиях препаратов инсулина весьма низка, что приводит к большому числу ошибок в инсулинотерапии. Между тем ориентироваться в препаратах инсулина должен врач любой специальности, поскольку до 3-4% населения в целом и до 10-30% пациентов стационара страдают сахарным диабетом.
Препараты инсулина отличаются друг от друга по степени очистки; источнику получения (бычий, свиной, человеческий); веществам, добавляемым к раствору инсулина (удлиняющим его действие, бактериостатикам и т.д.); концентрации; величине рН; возможности смешивания ИКД с ИПД.
Строение, изготовление и очистка
Инсулин – двухцепочечный белок с молекулярной массой около 5750 дальтон, состоящий из 51 аминокислоты. Предшественником инсулина является про-инсулин, в котором обе инсулиновые цепочки скреплены молекулой соединительного пептида (С-пептида). Годовая потребность в инсулине в мире составляет около 65 миллиардов единиц (1 единица = 42 мкг чистого вещества), поэтому производство инсулина требует высокотехнологичных способов его массового изготовления.
Раньше инсулин экстрагировали из поджелудочных желез крупного рогатого скота или свиней кислотно-спиртовым методом с последующей нейтрализацией и высаливанием; полученный таким образом препарат содержал лишь 89-90% инсулина. Повторным растворением и рекристаллизацией содержание инсулина увеличивали до > 90% (обычная степень очистки).
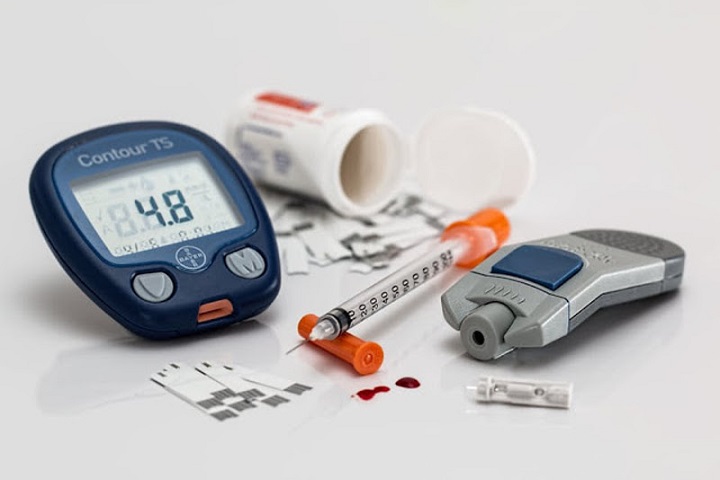 Для улучшения очистки инсулина далее его подвергают хроматографии. После однократной хроматографии препарата, предварительно прошедшего первичную очистку методом кристаллизации, получают так называемые монопиковые инсулины (помимо инсулина они содержат монодезаминоинсулин, моноаргинининсулин и моноэтилинсулин). После многократной хроматографии удается очистить инсулин до такой степени, при которой никаких примесей практически не остается – эти инсулины называются монокомпонентными (как правило, имеют маркировку на флаконе – МС). Сегодня необходимо стремиться к применению только препаратов инсулина высокой степени очистки: образование циркулирующих антител к инсулину (в конечном итоге снижающих его активность) и местные реакции при их использовании отмечаются значительно реже.
Для улучшения очистки инсулина далее его подвергают хроматографии. После однократной хроматографии препарата, предварительно прошедшего первичную очистку методом кристаллизации, получают так называемые монопиковые инсулины (помимо инсулина они содержат монодезаминоинсулин, моноаргинининсулин и моноэтилинсулин). После многократной хроматографии удается очистить инсулин до такой степени, при которой никаких примесей практически не остается – эти инсулины называются монокомпонентными (как правило, имеют маркировку на флаконе – МС). Сегодня необходимо стремиться к применению только препаратов инсулина высокой степени очистки: образование циркулирующих антител к инсулину (в конечном итоге снижающих его активность) и местные реакции при их использовании отмечаются значительно реже.
Виды препаратов по источнику получения
Инсулин свиньи и быка отличается от человеческого по аминокислотному составу: бычий – по трем аминокислотам, а свиной – по одной. Неудивительно, что при лечении бычьим инсулином побочные реакции развиваются гораздо чаще, чем при терапии свиным или человеческим инсулином. Эти реакции выражаются в иммунологической инсулинорезистентности, аллергии к инсулину, липодистрофиях (изменении подкожножировой клетчатки в месте инъекции).
Несмотря на явные недостатки бычьего инсулина, он все еще широко используется в мире, прежде всего в развивающихся странах, большим количеством больных, поскольку благодаря избытку сырья производство его обходится недорого. И все же недостатки бычьего инсулина в иммунологическом плане столь очевидны, что его ни в коем случае не рекомендуется назначать больным впервые выявленным сахарным диабетом, беременным или для кратковременной инсулинотерапии, например в периоперационном периоде. Отрицательные качества бычьего инсулина сохраняются и при использовании его в смеси со свиным, поэтому смешанные (свиной+бычий) инсулины также не стоит использовать для терапии указанных категорий больных.
Препараты инсулина человека по химической структуре полностью идентичны человеческому инсулину. В принципе, инсулин человека можно производить четырьмя способами:
- полным химическим синтезом;
- экстракцией из поджелудочных желез человека (оба этих способа не подходят из-за неэкономичности: недостаточной разработанности первого способа и недостатка сырья для массового производства вторым способом);
- полусинтетическим методом с помощью ферментно-химической замены в положении 30 В-цепи аминокислоты аланина в свином инсулине на треонин;
- биосинтетическим способом по генноинженерной технологии. Два последних метода позволяют получить человеческий инсулин высокой степени очистки.
Преимущество полусинтетического метода в том, что исходное вещество (свиной инсулин) получают и очищают давно и хорошо известными и усовершенствованными способами. Появлению вторичных примесей после ферментно-химической обработки можно воспрепятствовать соответствующим контролем качества. Недостаток полусинтетического метода заключается в постоянной зависимости производства от исходного сырья – свиного инсулина. При биосинтетическом производстве человеческого инсулина необходимый геномный материал переносят в микроорганизмы, которые начинают синтезировать предшественники инсулина.
Современные технологии на фирмах “Хехст” (Германия), “Эли Лилли” (США) и “Ново Нордиск” (Дания) – это три крупнейших мировых производителя инсулина – отличаются друг от друга по патентно-правовым аспектам. “Эли Лилли”, первая фирма, которая приступила к использованию генноинженерной технологии производства инсулина, с 1987 г. работает на человеческом геноме. С его помощью кишечная палочка (E.coli) синтезирует проинсулин, который после ферментного отщепления С-пептида превращается в инсулин (примеры – препараты Хумулин-Р, Хумулин-цинк, Хумулин-Н).
“Ново Нордиск” применяет синтетически полученную ДНК для “мини-про-инсулина”, то есть такого проинсулина, в котором С-пептид значительно короче, чем в проинсулине человека. Эту синтетическую ДНК вводят в дрожжевые микроорганизмы, которые начинают синтезировать “мини-проинсулин”, из которого потом ферментным способом выделяют инсулин, по аминокислотной последовательности соответствующий человеческому (примеры – Актрапид-НМ, Протафан-НМ и Актрафан-НМ).
Основной проблемой биосинтетическиго метода получения инсулина человека является полная очистка конечного продукта от малейших примесей использованных микроорганизмов и продуктов их жизнедеятельности. Новые методы контроля качества гарантируют, что биосинтетические инсулины человека вышеперечисленных производителей свободны от каких-либо вредных примесей; таким образом, их степень очистки и сахароснижающая эффективность отвечают самым высоким требованиям и являются практически одинаковыми. Каких-либо нежелательных побочных действий, зависящих от примесей, эти препараты инсулина не имеют.
Концентрация
Первые препараты инсулина содержали лишь 1 единицу инсулина в 1 мл. Позже их концентрация была увеличена. Большинство препаратов, использующихся в России, содержат 40 единиц инсулина в 1 мл (U-40). Однако во многих странах применяется инсулин, содержащий 100 единиц в 1 мл (U-100). Целесообразность перехода к U-100-инсулину у нас в стране пока вызывает сомнения.
Проблемы возникают уже сейчас, когда часть больных стала пользоваться инъекторами инсулина (шприц-ручками), в которых применяются специальные картриджи (пенфиллы) с инсулином U-100. В случае поломки шприца-ручки некоторые больные набирают U-100-инсулин из пенфиллов инсулиновыми шприцами, предназначенными для инсулина U-40 (и градуированными именно на эту концентрацию).
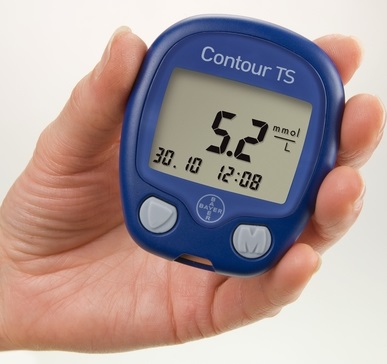 Практически никто из больных (да и многие врачи) не отдают себе отчета в том, что градуировка шприцев на единицы инсулина есть не что иное, как градуировка по объему раствора, рассчитанная именно на U-40-инсулин: 4 ед инсулина соответствуют 0,1 мл раствора, 6 ед – 0,15 мл и так далее, вплоть до 40 единиц, соответствующих 1 мл раствора (еще раз подчеркнем: при концентрации инсулина 40 ед/мл!). Если в такой шприц набрать инсулин с концентрацией 100 ед/мл до метки, например, 20 единиц, то получится, что в набранном объеме (0,5 мл) содержится уже 100 ед/мл х 0,5 = 50 единиц инсулина! Таким образом, набирая U-100-инсулин в обычные инсулиновые шприцы и ориентируясь при этом на метки “единиц”, мы всякий раз будем набирать дозу (100 ед/мл: 40 ед/ мл), превышающую в 2,5 раза ту, что отмечена возле данного деления шприца. Если больной или врач вовремя не обратят внимание на эту ошибку, возможны случаи тяжелых гипогликемий из-за передозировки инсулина, что мы неоднократно и наблюдали на практике.
Практически никто из больных (да и многие врачи) не отдают себе отчета в том, что градуировка шприцев на единицы инсулина есть не что иное, как градуировка по объему раствора, рассчитанная именно на U-40-инсулин: 4 ед инсулина соответствуют 0,1 мл раствора, 6 ед – 0,15 мл и так далее, вплоть до 40 единиц, соответствующих 1 мл раствора (еще раз подчеркнем: при концентрации инсулина 40 ед/мл!). Если в такой шприц набрать инсулин с концентрацией 100 ед/мл до метки, например, 20 единиц, то получится, что в набранном объеме (0,5 мл) содержится уже 100 ед/мл х 0,5 = 50 единиц инсулина! Таким образом, набирая U-100-инсулин в обычные инсулиновые шприцы и ориентируясь при этом на метки “единиц”, мы всякий раз будем набирать дозу (100 ед/мл: 40 ед/ мл), превышающую в 2,5 раза ту, что отмечена возле данного деления шприца. Если больной или врач вовремя не обратят внимание на эту ошибку, возможны случаи тяжелых гипогликемий из-за передозировки инсулина, что мы неоднократно и наблюдали на практике.
В последнее время в нашу страну по каналам гуманитарной помощи попадали инсулиновые шприцы, предназначенные для U-100-инсулина и градуированные именно для него. По ошибке в эти шприцы можно набрать из флаконов привычный нам U-40-инсулин, и тогда доза инсулина в шприце, рассуждая аналогично, однако “в обратную сторону”, окажется в 2,5 раза меньше той, что указана возле соответствующего деления шприца. Как следствие этого, можно ожидать “необъяснимое” повышение сахара крови – необъяснимого, впрочем, если не знать следующего правила: ддя каждой концентрации инсулина – соответствующий шприц!
Тщательно продуманный план, по которому осуществляли переход на U-100-инсулин, например в Швейцарии, может служить образцом. Однако он требует тесного взаимодействия и обучения всех участвующих сторон: больных, врачей, фармацевтов, промышленности и администрации.
рН инсулинового раствора
Некоторые препараты инсулина выпускаются в растворах с кислым рН (например, таким был отечественный препарат “инсулин для инъекций”, или “простой инсулин”; Депот-инсулин S, Депот-инсулин CR, Комб-инсулин и Комб-инсулин S, Германия). Кислые инсулины дают гораздо более выраженные иммунологические реакции на экзогенный инсулин и повышенную частоту реакций местной непереносимости. В настоящее время от применения препаратов инсулина с кислым рН практически отказались.
Смешивание инсулинов короткого и продленного действия
Современная инсулинотерапия, особенно при сахарном диабете I типа, обычно предусматривает применение как ИКД, так и ИПД. Больным было бы удобнее, если бы препараты ИКД и ИПД можно было смешивать в одном шприце и вводить одновременно, делая не два прокола кожи, а один. Предпосылкой терапии такого рода служит наличие химической и галеновой (т.е. зависящей от состава) сочетаемости ИКД и ИПД.
Особенно важно то, чтобы при смешивании ИКД и ИПД не растягивалось и не пропадало быстрое начало действия ИКД. Доказано, что ИКД можно смешивать в одном шприце с изофанным НПХ-инсулином, при этом быстрое начало действия ИКД не тормозится. Смеси этих инсулинов можно хранить.
Что касается препаратов ИЦС, то уже давно было известно, что кристаллическую ИЦС нельзя смешивать с ИКД, поскольку избыток цинка превращает ИКД в ИПД – по крайней мере, частично. Это доказано для Ультратарда. Если набрать в один шприц смесь Актрапида-НМ (ИКД) с Монотардом-НМ (ИПД) и сразу ввести ее под кожу, биодоступность ИКД уменьшается, поэтому начало его действия наступает позже, чем при раздельном введении этих препаратов. Поэтому смешивать Актрапид-НМ с Монотардом-НМ тоже нельзя.
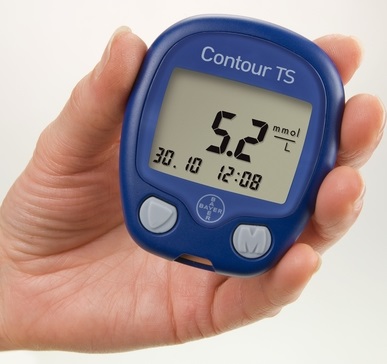 Некоторые больные вначале вводят ИКД, а затем, оставив иглу под кожей и слегка изменив ее направление, через нее же вводят цинк-инсулин. Хотя научных исследований по этому способу проводилось мало, нельзя исключить, что в части случаев и при таком введении под кожей образуется смесь ИКД с цинк-инсулином, что нарушит всасывание первого компонента. Поэтому мы рекомендуем совершенно раздельное введение ИКД и цинк-инсулина (в виде двух отдельных инъекций в участки кожи, отстоящие друг от друга не менее чем на 1 см; понятно, что это менее удобно, чем применение протамин-инсулина в одном шприце с ИКД).
Некоторые больные вначале вводят ИКД, а затем, оставив иглу под кожей и слегка изменив ее направление, через нее же вводят цинк-инсулин. Хотя научных исследований по этому способу проводилось мало, нельзя исключить, что в части случаев и при таком введении под кожей образуется смесь ИКД с цинк-инсулином, что нарушит всасывание первого компонента. Поэтому мы рекомендуем совершенно раздельное введение ИКД и цинк-инсулина (в виде двух отдельных инъекций в участки кожи, отстоящие друг от друга не менее чем на 1 см; понятно, что это менее удобно, чем применение протамин-инсулина в одном шприце с ИКД).
При смешивании с сурфен-инсулинами или неизофанными НПХ-инсулинами ИКД частично или полностью превращается в ИПД, поэтому приготовление подобных смесей нецелесообразно. В нашей стране отношение к смешиванию препаратов инсулина прошло два этапа. Вначале многие смешивали в одном шприце любые препараты инсулина, не зная об их особенностях. Затем перешли к другой крайности, вообще отказавшись от смешивания ИКД с ИПД и вводя их только раздельно, тем самым количество инъекций (проколов кожи) удваивалось. По-видимому, необходимо активнее доводить информацию о возможности смешивания ИКД и изофанного НПХ-инсулина до тех больных, которые ими пользуются.
Выпускаются и так называемые комбинированные инсулины – комбинации ИКД с НПХ-инсулинами в фиксированном процентном соотношении. Наиболее оправдывают себя смеси, содержащие 30% простого и 70% НПХ-инсулина, например инсулин Микстард и Актрафан-НМ (Ново Нордиск), Профиль III (Эли Лилли) или 25% простого и 75% НПХ-исулина, например Депот-Н-инсулин (Хехст). Однако такие комбинированные препараты больше подходят для больных, которым свойственны постоянный образ жизни, режим питания и двигательной активности (например, для пожилых больных сахарным диабетом II типа), так как они неудобны для проведения современной “гибкой” инсулинотерапии с частым изменением дозы ИКД при относительно мало меняющейся дозе ИПД.
Какие препараты инсулина лучше применять?
 Собственно говоря, для эффективной инсулинотерапии требуется лишь один препарат ИКД и один препарат ИПД, которые можно было бы смешивать друг с другом, а также – в основном для пожилых больных – препарат инсулина комбинированного действия. Согласно современным рекомендациям, следует использовать препараты инсулина, соответствующие следующим критериям: высокая степень очистки; нейтральный рН; возможность смешивания ИКД и ИПД. Из группы ИПД желательно применять препараты с продолжительностью действия 12-18 часов, подходящие для двукратного введения в сутки. Препараты типа Семиленте и Ленте в развитых странах практически не используются: первые – из-за недостаточной продолжительности действия (менее 10 часов), вторые – из-за наличия в них бычьего инсулина и невозможности смешивания в одном шприце с ИКД.
Собственно говоря, для эффективной инсулинотерапии требуется лишь один препарат ИКД и один препарат ИПД, которые можно было бы смешивать друг с другом, а также – в основном для пожилых больных – препарат инсулина комбинированного действия. Согласно современным рекомендациям, следует использовать препараты инсулина, соответствующие следующим критериям: высокая степень очистки; нейтральный рН; возможность смешивания ИКД и ИПД. Из группы ИПД желательно применять препараты с продолжительностью действия 12-18 часов, подходящие для двукратного введения в сутки. Препараты типа Семиленте и Ленте в развитых странах практически не используются: первые – из-за недостаточной продолжительности действия (менее 10 часов), вторые – из-за наличия в них бычьего инсулина и невозможности смешивания в одном шприце с ИКД.
С тех пор, как в распоряжении врача есть одновременно и человеческий, и высокоочищенный свиной инсулин, возникает вопрос: нужно ли вообще использовать последний. Установлено, что терапия полусинтетическим и биосинтетическим инсулином человека надежна и не сопряжена с побочными действиями, которые можно было бы отнести к способу получения препаратов. По сравнению с бычьим, инсулин человека обладает преимуществами вследствие незначительной антигенности. Однако по сравнению с высокоочищенными свиными инсулинами это преимущество инсулина человека выражено гораздо меньше и не является точно доказанным.
Важно!Иммунологические исследования больных, которые либо с самого начала получали человеческий инсулин, либо были переведены на него в процессе лечения, показали, что при подкожном введении инсулина человека также образуются циркулирующие антитела к инсулину. Это явление, поначалу весьма удивившее диабетологов, объясняют тем, что при подкожном введении происходит локальное энзиматическое разрушение инсулина, образующиеся фрагменты которого могут являться аллергенами.
В любом случае, проявления и степень иммунной реакции при лечении человеческим инсулином весьма незначительны. Как при лечении впервые выявленных больных, так и при переводе с других препаратов инсулин человека выгодно отличается от бычьего.
Однако различия в сахароснижающем действии между человеческим и свиным монокомпонентным инсулином отсутствуют, в иммунологическом отношении – невелики, а по данным некоторых исследований, и вовсе минимальны: антитела к инсулину в том и в другом случае образуются примерно в 5-8% случаев. Строго говоря, перевод на инсулин человека абсолютно показан в случаях иммунологической инсулинорезистентности или аллергии и при местной непереносимости свиного инсулина; при лечении больных впервые выявленным сахарным диабетом I типа; при необходимости временной инсулинотерапии (например, при операции).
 Большой ошибкой будет считать, что можно улучшить компенсацию обмена веществ, в том числе решить проблему так называемого лабильного диабета только за счет перевода больного со свиного на человеческий инсулин. От надежд такого рода больного (и врача) следует настойчиво предостеречь: они не имеют под собой никаких оснований.
Большой ошибкой будет считать, что можно улучшить компенсацию обмена веществ, в том числе решить проблему так называемого лабильного диабета только за счет перевода больного со свиного на человеческий инсулин. От надежд такого рода больного (и врача) следует настойчиво предостеречь: они не имеют под собой никаких оснований.
В 1990-91 гг. мы проанализировали эффективность использования различных видов инсулина в случайной выборке из 120 больных сахарным диабетом I типа. При этом оказалось, что при лечении препаратами как человеческого инсулина, так и инсулина животного происхождения интегральный показатель углеводного обмена за последние 3 месяца (гликированный гемоглобин, или НbА1) свидетельствовал о выраженной декомпенсации (о среднем уровне гликемии около 15-16 ммоль/л). После этого больные прошли специальную программу обучения, начали проводить самоконтроль глюкозы крови и научились самостоятельно изменять дозу инсулина; им было предоставлено самим выбирать, какими препаратами инсулина пользоваться. Через год у всех больных произошло значительное улучшение компенсации углеводного обмена, и опять она не зависела от пида инсулина.
Аналогичным образом отсутствовала и разница в средней потребности в инсулине на килограмм массы тела – как исходно, так и в динамике. Нисколько не желая умалить достоинств инсулина человека в иммунологическом плане, мы лишь хотим продемонстрировать, что сам по себе он не является ни необходимым, ни достаточным для достижения хорошей компенсации углеводного обмена. О чем нужно помнить при переводе на инсулин человека? У больных, которые на фоне лечения инсулином животного происхождения имели высокий титр антител к инсулину, в течение месяцев после перевода на человеческий инсулин титр антител снижается, поэтому длительность действия инсулина может укорачиваться, а максимальный сахаросодержащий эффект – несколько усиливается.
 Человеческий ИКД начинает действовать несколько быстрее, чем свиной. При переводе на инсулин человека больных следует информировать об этих возможных изменениях времени действия инсулина. Важно, чтобы больной вводил инсулина не больше, чем нужно; при этом необходимо регулярно удостоверяться в том, нельзя ли достичь хорошей компенсации на меньшей дозе инсулина, особенно ИПД. Но столь же важно и обратное: доза инсулина не должна быть меньше той, которая необходима конкретному больному для хорошей компенсации.
Человеческий ИКД начинает действовать несколько быстрее, чем свиной. При переводе на инсулин человека больных следует информировать об этих возможных изменениях времени действия инсулина. Важно, чтобы больной вводил инсулина не больше, чем нужно; при этом необходимо регулярно удостоверяться в том, нельзя ли достичь хорошей компенсации на меньшей дозе инсулина, особенно ИПД. Но столь же важно и обратное: доза инсулина не должна быть меньше той, которая необходима конкретному больному для хорошей компенсации.
Распространено мнение, что после перевода с инсулина животного происхождения на инсулин человека доза препарата должна быть уменьшена из-за возможных гипогликемий. Это верно лишь для тех больных, у которых исходно был высокий титр антител к инсулину, частично связывающих экзогенный инсулин животного происхождения и, следовательно, снижающих уровень свободного (т.е. активно действующего) инсулина в плазме. Человеческий инсулин этими антителами не связывается или связывается в очень небольшой степени. Кроме того, титр антител после перевода на инсулин человека с течением времени падает; все это ведет к тому, что уровень свободного инсулина становится выше, чем имелся при той же дозе инсулина животного происхождения, а это может сопровождаться появлением гипогликемий.
Однако если больной до перевода на человеческий инсулин не имел высокого титра антител к инсулину, то ожидать снижения дозы нет никаких оснований. Второй важный фактор, влияющий на возможное снижение дозы инсулина, – степень гипергликемии. У длительно декомпенсированных больных развивается временное снижение чувствительности к экзогенному инсулину (теория “глюкозной токсичности”).
«12817»]
Если в это время пытаться компенсировать их с помощью инсулина животного происхождения, потребуется существенное увеличение дозы. Если же перевести их на инсулин человека в прежней дозе, то, согласно описанному выше механизму, уровень свободного инсулина станет выше, произойдет как бы относительное увеличение дозы “внутри” организма больного, что и позволит улучшить компенсацию. Если же дозу инсулина человека снизить сразу, не ожидая снижения гликемии и появления легких гипогликемий, то уровни свободного инсулина в этом случае окажутся недостаточными для преодоления исходной декомпенсации и преимуществ от перевода на инсулин человека не будет получено.
К сожалению, это и происходит у очень многих больных, когда врачи, в отсутствие возможности определить уровень антител, выполняют ошибочную устаревшую инструкцию, которая гласит: при переводе на инсулин человека следует сразу уменьшить дозу инсулина на 25%. Как же поступать с дозой инсулина человека на практике? Нужно руководствоваться двумя моментами: а) коррекцию дозы инсулина в любую сторону проводят только в соответствии с реальным уровнем гликемии; снижение дозы требуется лишь после появления легких гипогликемий; б) потребность в инсулине может снизиться у разных больных в разное время – как сразу после перевода, так и лишь через несколько недель или месяцев, но может и не снизиться вообще.
Фармакокинетика подкожно введенного инсулина
 После инъекции инсулин может оказать сахароснижающее действие только после того, как он достигнет тканей-мишений (в первую очередь печени, мышц и жировой ткани), а для этого он должен всосаться из подкожной клетчатки в кровь. Молекулярно-биологические механизмы всасывания инсулина в кровоток после подкожного введения не ясны окончательно и по сей день. Сейчас, когда уже доказано, что целью лечения больных сахарным диабетом с большой ожидаемой продолжительностью предстоящей жизни является (почти) нормогликемия, все яснее становится роль как можно более постоянной, предсказуемой абсорбции подкожно введенного инсулина как одной из важнейших предпосылок успеха лечения.
После инъекции инсулин может оказать сахароснижающее действие только после того, как он достигнет тканей-мишений (в первую очередь печени, мышц и жировой ткани), а для этого он должен всосаться из подкожной клетчатки в кровь. Молекулярно-биологические механизмы всасывания инсулина в кровоток после подкожного введения не ясны окончательно и по сей день. Сейчас, когда уже доказано, что целью лечения больных сахарным диабетом с большой ожидаемой продолжительностью предстоящей жизни является (почти) нормогликемия, все яснее становится роль как можно более постоянной, предсказуемой абсорбции подкожно введенного инсулина как одной из важнейших предпосылок успеха лечения.
При этом следует учитывать, что подкожное введение инсулина в принципе нефизиологично, поскольку оно осуществляется в место, не самое подходящее с анатомической и физиологической точки зрения. Основное действие инсулина в плане регуляции гомеостаза глюкозы разворачивается в печени; уже в процессе первого прохождения через печень инсулина, который образуется в поджелудочной железе и поступает в систему воротной вены, элиминируется примерно половина этого гормона, и лишь остальное количество попадает в периферическое кровообращение. В результате уровень инсулина в крови воротной вены существенно выше, чем на периферии.
При подкожном введении инсулина он вначале проходит по большому и малому кругам кровообращения и лишь затем по печеночным артериям достигает мишени – гепатоцитов. Понятно, что в этом случае для достижения физиологической концентрации инсулина в печени необходим гораздо более высокий уровень инсулина в периферической крови, чем это бывает у здорового человека. По этой причине при подкожном введении инсулина при сахарном диабете приходится считаться с наличием различной степени периферической гиперинсулинемии.
Другая проблема при подкожной инсулинотерапии заключается в изменении периода полужизни инсулина. У здорового человека период полужизни циркулирующего инсулина составляет около 4 минут. После всасывания подкожно введенного ИКД период жизни удлиняется примерно в 10 раз (до 40 минут). Период полужизни ИПД вполне может растянуться до нескольких часов. Это существенно нарушает гибкость “тонкой” регуляции гомеостаза глюкозы.
Внимание!С помощью фармакокинетических исследований удалось точно описать кинетику всасывания подкожно введенного ИКД. Высокоочищенные препараты свиного инсулина, а соответственно и препараты инсулина человека, всасываются очень быстро: уже через 10 минут после инъекции отмечается значительный подъем уровня инсулина в сыворотке. Примерно через 60 минут достигается плато биодоступности инсулина, а снижение уровня циркулирующего инсулина до исходных величин растягивается на несколько часов, в то время как в физиологических условиях уменьшение инсулинемии до базального уровня наблюдается в течение немногих минут после прекращения выброса инсулина.
Некоторая часть (не менее 10-20%) подкожно введенного инсулина подвергается энзиматическому расщеплению в месте инъекции еще до того, как он попадает в кровоток. Существует довольно редкая форма инсулинорезистентности, когда еще большая часть введенной дозы инсулина подвергается деградации в подкожной клетчатке. Эту особую форму инсулинорезистентности, при которой для достижения компенсации обмена веществ требуются астрономические количества инсулина, можно легко диагностировать по различию в сахароснижающем действии ИКД при подкожном и внутривенном введении.
Различия в процессе локальной деградации инсулина в зависимости от места инъекции, а также различия между больными играют определенную роль в том, что добиться стабильного уровня сахара крови при подкожной заместительной инсулинотерапии достаточно трудно. Не вполне ясны и механизмы дальнейшего транспорта инсулина на его пути от места подкожного введения в кровоток. Более 80% введенного ИКД проходит прямо в кровеносные капилляры, и лишь очень небольшая и непостоянная часть его попадает в кровоток через лимфатические пути. Возможно, изменения базальных мембран и эндотелия сосудов при диабетических микроангиопатиях небезразличны для процесса всасывания инсулина.
Физико-химические основы всасывания ИПД до сих пор практически не определены; выявлена существенная вариабельность кинетики всасывания у разных больных.
Факторы, влияющие на всасывание
Место инъекции
 Кинетика всасывания подкожно введенного ИКД зависит от анатомического строения места инъекции. Это особенно заметно при патологических изменениях подкожножировой клетчатки, например липодистрофиях. Введение инсулина в измененные участки кожи сопровождается непредсказуемыми колебаниями его всасывания, поэтому инъекций в такие участки следует избегать.
Кинетика всасывания подкожно введенного ИКД зависит от анатомического строения места инъекции. Это особенно заметно при патологических изменениях подкожножировой клетчатки, например липодистрофиях. Введение инсулина в измененные участки кожи сопровождается непредсказуемыми колебаниями его всасывания, поэтому инъекций в такие участки следует избегать.
Нам неоднократно приходилось сталкиваться и со случаями, когда и больной, и его врач были убеждены в “тяжести” диабета и инсулинорезистентности, что проявлялось в невозможности добиться компенсации даже на больших дозах человеческого инсулина. Простейший осмотр пациента позволял выявить причину: следы от инъекций располагались вплотную друг к другу на маленьком участке кожи диаметром не более 2-3 см, над уплотненным, утолщенным слоем подкожной клетчатки. При расспросе больных выяснилось, что они (или медицинские сестры!) неделями или месяцами вводили инсулин в этот участок.
Возникшие при этом изменения подкожножировой клетчатки существенно замедляют и уменьшают всасывание инсулина в кровоток, что снижает эффективность его действия. Смена места инъекции и соблюдение необходимого расстояния между отдельными проколами кожи (не менее 1 см) позволяют быстро ликвидировать мнимую инсулинорезистентность. Вследствие анатомических различий в плотности капилляров подкожного слоя в различных регионах тела даже при неизменной подкожножировой клетчатке инсулин всасывается по-разному.
Так, из области живота инсулин поступает в кровоток существенно быстрее, чем после введения его в область бедра; инъекция в плечо, которую предпочитают многие больные, по скорости всасывания инсулина занимает промежуточное положение. При нерегулярной и бессистемной смене мест инъекции от одной области тела к другой также могут возникнуть выраженные колебания сахароснижающего действия инсулина; так, эффект ИКД начнется раньше и будет более выражен при введении инсулина в область живота по сравнению с введением его в бедро.
 Вот почему смена мест инъекции (живот – бедро – плечо) не должна быть хаотичной; место инъекции необходимо последовательно менять в пределах одной области по определенной схеме: например, утром всегда делать инъекцию в живот, в обед – в плечо, вечером – в бедро или же все инъекции – в область живота.
Вот почему смена мест инъекции (живот – бедро – плечо) не должна быть хаотичной; место инъекции необходимо последовательно менять в пределах одной области по определенной схеме: например, утром всегда делать инъекцию в живот, в обед – в плечо, вечером – в бедро или же все инъекции – в область живота.
Температура
Особенно заметные изменения всасывания инсулина можно наблюдать при изменении температуры кожи в месте инъекции. Так, горячая ванна или прикладывание горячей грелки резко ускоряет абсорбцию инсулина, а после холодной ванны всасывание надолго тормозится. Указанные эффекты выражены настолько сильно, что могут клинически значимо влиять на компенсацию углеводного обмена.
Так, летом пребывание под палящим солнцем приводит не только к солнечным ожогам, но и к значительному ускорению всасывания инсулина и, как следствие, гипогликемиям, о чем следует предупреждать больных. Напротив, сауна, в отличие от прежних предположений о ней, очевидно, не вызывает никакого заметного ускорения всасывания инсулина. Вероятно, здесь накладывается друг на друга действие различных, противоположных друг другу факторов.
Не рекомендуется вводить инсулин, только что вынутый из холодильника (медленное всасывание). Раствор инсулина должен иметь комнатную температуру, поэтому начатый флакон лучше хранить вне холодильника, в темном месте.
Массаж места инъекции
Самого сильного ускорения всасывания инсулина можно достичь путем легкого массажа места инъекции сразу же после введения. Опять-таки это надо делать либо постоянно, либо не делать совсем.
Мышечная работа
 При мышечной работе в определенных условиях может произойти выраженное ускорение действия инсулина. Длительное время это явление переоценивали в качестве возможной причины гипогликемии, возникающей при физической нагрузке. Дело доходило даже до того, что для профилактики гипогликемии на фоне мышечной работы больным рекомендовали вводить предшествующую нагрузке дозу инсулина в тот участок тела, который меньше всего или совсем не будет участвовать в работе. Однако эту рекомендацию нельзя считать разумной.
При мышечной работе в определенных условиях может произойти выраженное ускорение действия инсулина. Длительное время это явление переоценивали в качестве возможной причины гипогликемии, возникающей при физической нагрузке. Дело доходило даже до того, что для профилактики гипогликемии на фоне мышечной работы больным рекомендовали вводить предшествующую нагрузке дозу инсулина в тот участок тела, который меньше всего или совсем не будет участвовать в работе. Однако эту рекомендацию нельзя считать разумной.
Во-первых, видов физической активности, которые изолированно затрагивают только некоторые, определенные части тела, очень мало. Во-вторых, ускорение всасывания инсулина выражено существенно только тогда, когда физическая нагрузка на данный участок тела имеет место в пределах первого получаса после инъекции, что практически встречается довольно редко. В-третьих, показано, что усиление сахароснижающего действия физической нагрузки через 45 минут после введения ИКД совсем не зависит от того, куда был введен инсулин – в плечо или бедро, так как основной механизм действия физической нагрузки – усиление утилизации глюкозы тканями, а не ускорение всасывания инсулина.
Таким образом, рекомендация менять место инъекции перед мышечной работой для профилактики гипогликемий неэффективна. Именно в результате этой нецелесообразной рекомендации в последние годы были отмечены многочисленные случаи тяжелых гипогликемий у больных диабетом на фоне занятий спортом. Чтобы избежать гипогликемии при физической нагрузке, нужно прибегать к давно известным правилам: прием дополнительного количества углеводов (при кратковременной) и/или снижение дозы инсулина (при длительной мышечной работе).Глубина инъекции.
Часто забывают о такой причине непонятных колебаний сахара в крови, как случайное внутримышечное или внутрикожное введение инсулина. Сделанная по ошибке и оставшаяся незамеченной (ввиду своей безболезненности) внутримышечная инъекция возможна как раз при использовании современных тончайших и коротких инсулиновых игл. У худых больных слой подкожножировой клетчатки на участках тела, куда обычно делают инъекции инсулина, чаще всего гораздо тоньше 12 мм.
Внимание!Длина игл шприцев-ручек и одноразовых инсулиновых шприцев равняется 12-13 мм, поэтому, если вкалывать иглу перпендикулярно к поверхности кожи, в большинстве случаев инсулин будет введен внутримышечно. Такую “перпендикулярную” инъекцию часто делают именно те, кто пользуется шприцами-ручками, поскольку эта техника наглядно представлена на многих промышленно выпускаемых инструкциях. Чтобы обеспечить по возможности одинаковое, унифицированное всасывание инсулина из подкожножировой клетчатки, необходимо взять складку кожи и вколоть иглу под углом 45 градусов.
С другой стороны, внутримышечное введение инсулина упомянутыми иглами безболезненно и безопасно. Хорошо обученные больные могут успешно пользоваться этой техникой, например, перед приемом быстроусвояемых углеводов или в случае кетоацидотической декомпенсации, чтобы ускорить действие ИКД. После внутримышечного введения инсулина в плечо или бедро он всасывается значительно быстрее, чем после подкожного. При введении в область живота различия между подкожной и внутримышечной инъекцией выражены меньше. Однако внутримышечное введение препаратов ИПД не рекомендуется из-за укорочения продолжительности действия и усиления нежелательных колебаний активности.
 При случайном внутрикожном введении (что бывает, если иглу вкалывают под слишком малым углом к коже или неглубоко) инсулин всасывается плохо, а в месте инъекции может возникать покраснение и болезненность, которые иногда ошибочно трактуются как аллергия.
При случайном внутрикожном введении (что бывает, если иглу вкалывают под слишком малым углом к коже или неглубоко) инсулин всасывается плохо, а в месте инъекции может возникать покраснение и болезненность, которые иногда ошибочно трактуются как аллергия.
Доза инсулина
Доказано, что продолжительность действия инсулина зависит от введенной разовой дозы (см. таблицу 2). После подкожного введения Актрапида в дозе 0,1 ед/кг достоверное повышение инсулинемии наблюдается на протяжении 4-6 часов; при повышении дозы до 0,2 ед/кг удваивается не только активность, но и продолжительность действия инсулина. Иными словами, при введении 6 ед ИКД больному весом 60 кг активное сахароснижающее действие будет проявляться, как правило, в течение 4 часов (редко – дольше, так как не всегда незначительно повышенный уровень инсулина в крови оказывает существенное влияние на гликемию); введение этому же больному 12 ед ИКД будет сопровождаться сахароснижающим эффектом примерно до 7 часов. Не следует забывать при этом, что переваривание большинства блюд (независимо от съеденного количества) заканчивается через 4-6 часов!
Таким образом, инсулин как лекарственное средство уникален в том отношении, что его клиническая эффективность зависит не только и, может быть, не столько от характеристик препаратов как таковых, но и – в огромной степени! – от многочисленных факторов, связанных с обращением с препаратами и техникой введения.
Не будет преувеличением утверждение, что значительный процент случаев так называемого лабильного диабета, то есть нерегулярных и непредсказуемых колебаний сахара крови при сахарном диабете I типа, на самом деле не является каким-то клиническим вариантом течения заболевания, а развивается вследствие недостаточного знания вышеописанных феноменов и их неучета при проведении инсулинотерапии. О факторах, влияющих на фармакокинетику инсулина, и особенностях различных препаратов необходимо информировать больных при обучении. Врач и больной должны учитывать возможные отклонения длительности и силы действия препаратов инсулина от традиционных схем и стараться выработать индивидуальную инсулинотерапию, а не следовать жесткому плану, который вряд ли приведет к успеху по вышеупомянутым причинам.
Инсулин применяется в лечении сахарного диабета почти 90 лет. За это время появилось много новых методов введения инсулина больным. В настоящее время пациенты могут выбирать между традиционными шприцами с иглами, инсулиновым шприцом, а также инсулиновым насосом. О выборе метода приема инсулина следует проконсультироваться с врачом.
Традиционные инъекции
 Несмотря на то, что в последние годы появились более современные методы приема инсулина, наибольшей популярностью среди больных диабетом пользуются инъекции. Введение инсулина с помощью шприца и иглы не представляет большой проблемы для пациента. Достаточно загрузить нужную дозу инсулина в капсулу и ввести в подкожную клетчатку.
Несмотря на то, что в последние годы появились более современные методы приема инсулина, наибольшей популярностью среди больных диабетом пользуются инъекции. Введение инсулина с помощью шприца и иглы не представляет большой проблемы для пациента. Достаточно загрузить нужную дозу инсулина в капсулу и ввести в подкожную клетчатку.
Интересным решением для людей, больных диабетом, которые имеют проблемы со зрением, направляющие иглы – устройства, которые помогают поддерживать шприц в нужном месте и под прямым углом во время инъекции инсулина. Некоторые из этих устройств имеют в комплекте увеличительное стекло, благодаря чему люди, плохо видящие в состоянии прочитать небольшие надписи на игле.
Аксессуары, облегчающие введение инсулина имеют большое значение в лечении сахарного диабета, ибо эта болезнь является основной причиной потери зрения у людей между 20 и 74 годами.
Современные методы введения
Инъекции инсулина для больных диабетом – неприятный долг, поэтому ученые давно уже работают над устройствами, которые могли бы облегчить его введение. Хорошим примером инновационного решения являются устройства, предназначенные для наполнения шприца инсулином. Они в состоянии отмерить нужную дозу инсулина, а также, в случае необходимости, смешивать два различных типа инсулина.
Настоящим прорывом в приеме инсулина стали так называемые инсулиновые ручки. Эти устройства, напоминающие с виду большие шариковые ручки оснащены механизмом с иглой и системой отмеривания дозы инсулина. Для того, чтобы ввести его под кожу, достаточно установить желаемую дозу и нажать на кнопку. Перед каждым использованием необходимо менять иглу на новую. Когда „картридж” с инсулином заканчивается, его также меняют на новый.
Такой инструмент является отличным выбором для людей, которые сталкиваются с проблемами со зрением. Устройства этого типа издают звук при определении дозы, благодаря чему пациент с амблиопией может самостоятельно отмерить дозу инсулина и вводили ее без посторонней помощи.
Совет!Альтернативой являются безыгольные инжекторы инсулина. Эти устройства под высоким давлением вдавливают инсулин под кожу. Несмотря на то, что безыгольные инжекторы представляются идеальным решением, некоторые люди, страдающие сахарным диабетом, считают, что их применение является более болезненным, чем тех же игл.
Выполнение инъекции инсулина обременительно, поэтому были разработаны дозаторы инсулина. Это оборудование подает инсулин в течение всего дня. Инсулиновые насос подключается к небольшой трубке или катетеру с иглой, которая введена под кожу, чаще всего, на животе больного. Насос размером с колоду карт и его можно запрограммировать таким образом, чтобы он вводил инсулин после еды.
Устройства этого типа постоянно вводят инсулин, но пациент может сам принять дозу после еды, чтобы сохранить низкий уровень сахара в крови. К сожалению, дозаторы инсулина не являются простыми в использовании. Как правило, рекомендуется использовать их в случае сахарного диабета 1 типа, но его могут использовать также больные сахарным диабетом 2 типа.
Работа над идеальным способом введения инсулина больным диабетом постоянно продолжаются. Существующие в настоящее время способы инъекции инсулина не идеальны, но каждый день помогают миллионам пациентов.